蛋白的高级结构决定其功能,行使功能需要正确折叠。蛋白由20多种不同氨基酸组成,需要折叠成正确的三维结构才能发挥自身作用。蛋白质在一定的物理和化学条件(加热、加压、脱水、振荡、紫外线照射、超声波、强酸、强碱、尿素、重金属盐、十二烷基硫酸钠)下,其空间构象容易发生改变而失活,因此研究蛋白的构象和构型变化对其应用有重要的价值。蛋白质的变性作用主要是由于蛋白质分子内部的结构被破坏。天然蛋白质的空间结构是通过氢键等次级键维持的,而变性后次级键被破坏,蛋白质分子就从原来有序的卷曲的紧密结构变为无序的松散的伸展状结构(但一级结构并未改变)。热变性是蛋白质变性中最常见的一类现象。
蛋白质变性温度是生物学家们研究蛋白质的热稳定性的一个重要的概念,是指蛋白质在特定温度条件下受到热力作用时,其结构发生变化的温度点,一般温度较高时,蛋白质从稳定的三维结构变化成松散的无序结构。蛋白质的热稳定性一般使用热变性中点温度(meltingtemperature,Tm)来表示,即蛋白质解折叠50%时的温度。蛋白质的热变性过程与其空间构象的改变密切相关,Tm值能反映变温过程中蛋白质构象改变的趋势,是衡量蛋白质热稳定性的一个重要指标。蛋白质Tm值的测定在生物医药行业具有广泛的应用,如嗜热蛋白、工业酶等的改造与筛选,蛋白质药物与配体、制剂或辅料的相互作用,蛋白质药物的缓冲液稳定条件筛选等。
蛋白由α螺旋和β折叠构成,α螺旋和β折叠在红外和紫外光段有特异的光吸收。蛋白质对左旋和右旋圆偏振光的吸收存在差异,利用远紫外区(190~260nm)的光谱特征能够快速分析出溶液中蛋白质的二级结构,进而分析和辨别出蛋白质的三级结构类型,变温过程中测量蛋白等物质的圆二色谱,能反映其随温度升高结构变化的趋势。此外,通过测定蛋白质在不同温度下的平均残基摩尔椭圆度[θ]可以获得蛋白质的Tm值。
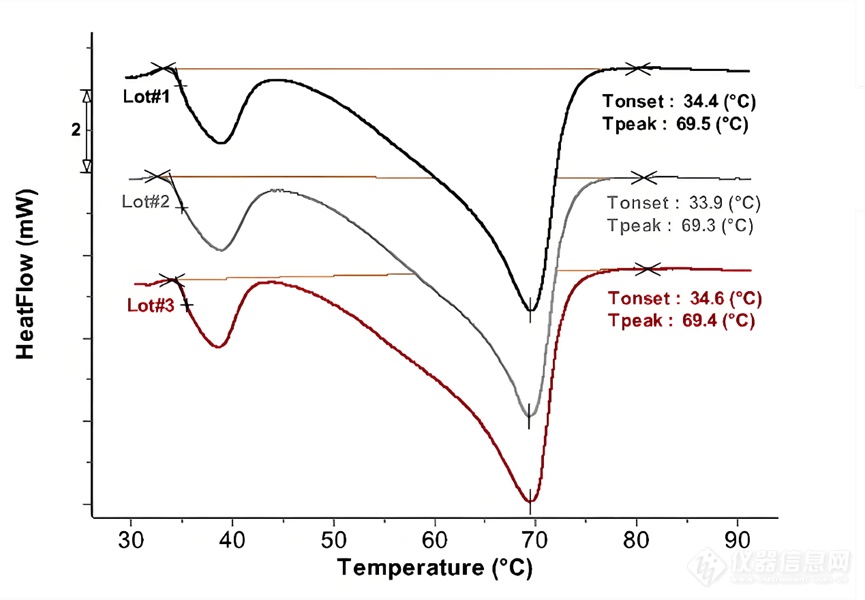
差示扫描量热法(DSC)是一个很经典的一个技术,基于的蛋白变性过程中对热量的吸收。蛋白是有三维结构的,比如氢键,疏水键,范德华力。一旦通过加热然后把结构破坏掉,需要吸收热量。所以可以测量热量变化,就是加热结构变化过程中的热量吸收。通过对参照物和样品同时进行升温或冷却处理,测定两者为保持相同温度所产生的热量差,从而计算蛋白质的Tm值。
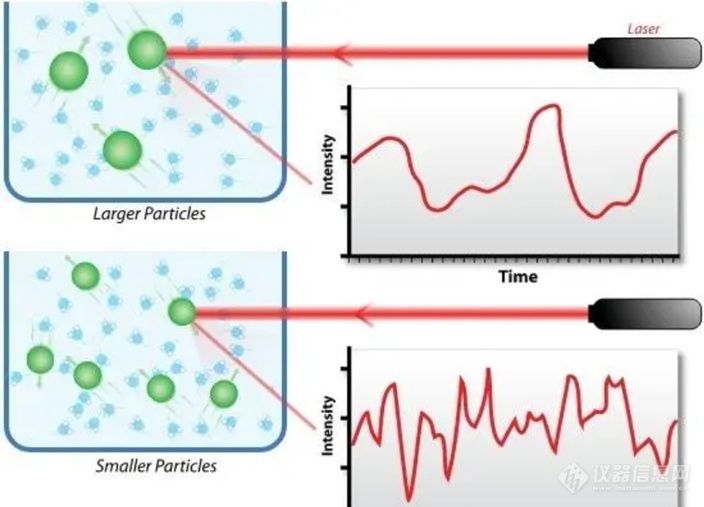
动态光散射是基于光学的方法,检测的是蛋白变性之后会发生聚集,导致颗粒的大小发生改变,对散射信号的影响。蛋白在变性过程中,从一个规则高级折叠结构打开,变成一个线性的松散结构。本来外部是亲水的氨基酸,内部是疏水的氨基酸。一旦打开之后,这些疏水的氨基酸会相互就是结合到一起。就是因为疏水的一个相互作用,然后变成一个球状聚集体。此过程会引起这个光的散射的变化。基于动态光散射的信号随着加热的过程的变化就代表粒径的变化,可以计算出蛋白质的Tm值。
动态光散射用于表征蛋白质、高分子、胶束、糖和纳米颗粒的尺寸。如果系统是单分散的,颗粒的平均有效直径可以求出来,这一测量取决于颗粒的心,表面结构,颗粒的浓度和介质中的离子种类。DLS也可以用于稳定性研究,通过测量不同时间的粒径分布,可以展现颗粒随时间聚沉的趋势。随着微粒的聚沉,具有较大粒径的颗粒变多。同样,DLS也可以用来分析温度对稳定性的影响。
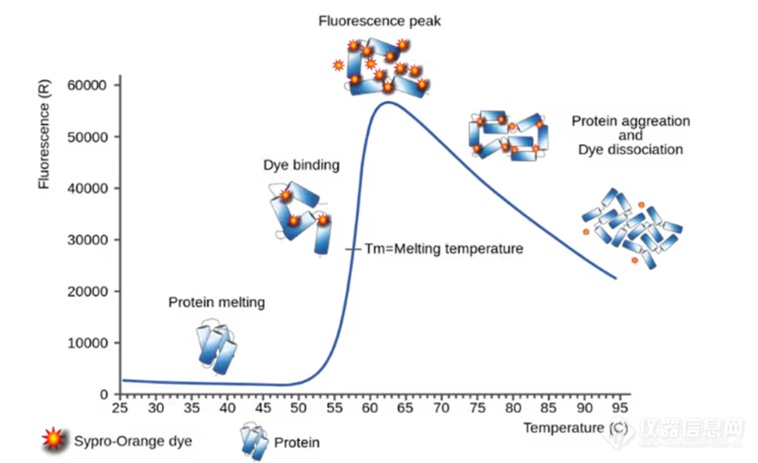
差示扫描荧光(DSF)也被称为热荧光法(ThermoFluor),是一种经济高效且易于使用的生物物理技术,通过检测当温度升高或变性剂存在时荧光发射光谱的相应变化来确定蛋白质的变性温度(热变性温度Tm值或化学变性Cm值)。Pantoliano等最先应用此技术测定了上百种蛋白质的热稳定性。差示扫描荧光法分为添加外源荧光染料与不添加荧光染料两种方式,都是利用加热使蛋白内部疏水基团暴露这一特点进行检测Tm值。
传统DSF经常使用350/330比值法来进行数据分析根据荧光源不同分为内源荧光DSF和外源荧光染料DSF。基于外源染料荧光的DSF其原理是利用能与蛋白内部疏水基团相互作用的染料为荧光源。蛋白质加热变性后疏水基团暴露,疏水基团与亲和性染料结合产生荧光信号,检测荧光强度变化测定蛋白质的Tm值。
特点:借助荧光定量PCR适用于高通量筛选,信号强度可控,灵敏度和准确性都较高。但添加的外源染料可能会对蛋白质结构和功能产生影响,且操作较复杂,不适用于所有蛋白研究。比如做膜蛋白研究时,溶液环境中需要添加双亲性的分子,一端疏水一端亲水。这种情况荧光分子会直接结合到疏水端,导致直接产生荧光信号。并且染料种类的选择、浓度的选择也很繁琐。外源荧光染料DSF也可能会产生背景荧光以及非特异吸附等假阳性结果。
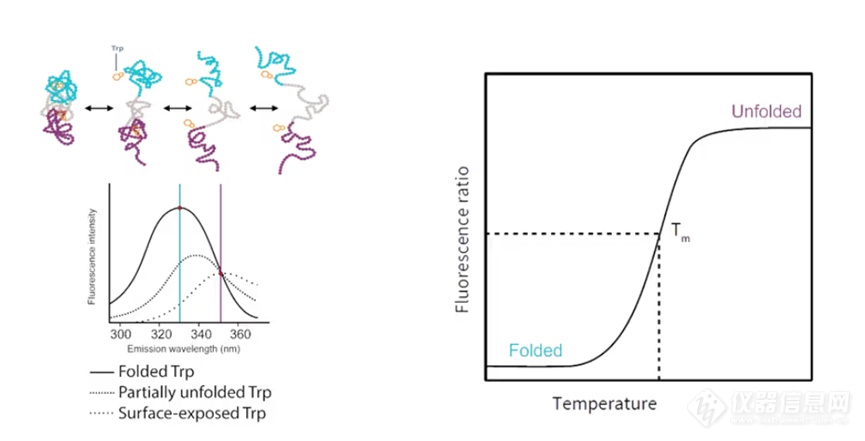
内源差式扫描荧光inDSF,基于蛋白质中特定氨基酸的荧光特性。这些氨基酸的荧光强度与其所处的微环境密切相关,因此,当蛋白质的结构发生变化时,这些氨基酸的荧光信号也会随之改变。不需要额外的荧光染料加入到检测体系中,利用蛋白内部芳香族氨基酸的自发光原理。不需要任何额外的标记或固定步骤,避免引入结果的不确定性。
研究发现,蛋白质分子中芳香环氨基酸在处于不同极性的微环境时(如疏水或亲水环境中),其被激发的内源荧光的最大发射光谱会发生位移。蛋白质中内源荧光主要来自含芳香环氨基酸如色氨酸(Trp),苯丙氨酸(Phe)和酪氨酸(Tyr),其中以色氨酸内源荧光最强。当它在蛋白内部时,发射光主要在330波段,当蛋白一旦去折叠,暴露在溶剂中,发出的光就会从330波长红移到350。所以通过280激发,检测330/350的比值变化,就能测量蛋白质的Tm值。以色氨酸为例,在蛋白质疏水的内核微环境中,其内源荧光最大发射波长在330nm左右,而在亲水的极性微环境中,色氨酸的内源荧光最大发射波长则出现在350nm左右。蛋白质热变性或者化学变性通常会导致色氨酸残基周围微环境的极性发生变化,使通常被包埋于蛋白质疏水内核的色氨酸逐渐暴露于亲水的环境中,从而导致发射内源荧光最大发射波长发生红移(RedShift),即向更大的波长区域移动。
总得来说,DSF和DLS法在样品用量及测定效率上更有优势,比较适合进行高通量筛选。但DSF法需要样品含有色氨酸、酪氨酸或额外添加荧光染料,这可能会对样品测量范围带来一定限制,DLS对样品浓度有要求。DLS还可以获取聚集体粒径大小的信息。DSC法虽然在样品用量与检测效率上不及DSF,但作为量热的经典方法仍是不可缺少的Tm值测量手段,在进行批量样品的热稳定性筛选时,可以使用DSF法初筛,DSC法复筛。此外,DSC能测定蛋白质变性过程中的热容变化ΔCp、焓变ΔH、解折叠自由能ΔG、玻璃态转变温度、分子流动临界温度等其他重要热力学参数。CD作为检测蛋白二级结构的经典方法,在Tm值测定方面具有其独特优势和一定的局限性,也是研究加热过程中蛋白结构改变的重要方法。
蛋白质Tm值测定具有重要的实际应用价值,例如辅助生物药物开发、生产和质量控制,评估生物相似性、优化蛋白药物配方等,还可以作为探索蛋白质高级结构的手段之一指导蛋白质工程,如比较不同突变对蛋白质稳定性的影响,研究结构域改变与功能活性改变关联性等。比较不同Tm值测定方法,全面了解技术特点及测量效果对于Tm值测定的实际应用具有一定的指导意义,在科研或生产工作中可以灵活选用或联用多种技术来阐明不同条件下的结构变化特点。
北京佰司特科技有限责任公司于2023-10-01日推出了自主研发的第一款国产蛋白稳定性分析仪,该设备性能和参数达到进口设备的水平,价格却远低于进口产品,弥补了目前国产自主设备在蛋白稳定性专业研究分析领域的空白。多功能蛋白稳定性分析仪PSA-16是一款无需荧光染料、高通量、低样品消耗量的检测蛋白质稳定性的设备。该设备基于内源差示扫描荧光技术(intrinsic fluorescence DSF),通过检测温度变化/变性剂浓度变化过程中蛋白内源紫外荧光的改变,获得蛋白质的热稳定性(Tm值)、化学稳定性(Cm值)等参数。可应用于蛋白缓冲液条件筛选及优化、小分子与蛋白结合情况的定性测定太阳成集团tyc45668cn、蛋白质修饰及改造后的稳定性测定、蛋白变/复性研究、不同批次间蛋白稳定性对比等多个方面。
多功能蛋白稳定性分析仪PSA-16应用涵盖植物、生物学、动物科学、动物医学、微生物学、工业发酵、环境科学、农业基础、蛋白质工程等多学科领域。蛋白质是最终决定功能的生物分子,其参与和影响着整个生命活动过程。现代分子生物学、环境科学、动医动科、农业基础等多种学科研究的很多方向都涉及蛋白质功能研究,以及其下游的各种生物物理、生物化学方法分析,提供稳定的蛋白质样品是所有蛋白质研究的先决条件。因此多功能蛋白稳定性分析仪PSA-16在各学科的研究中都有重要的意义。
全国首家新能源汽车检测国家示范站——郑州市三十里铺光储充检公交场站正式投入运营
华大九天“一种集成电路版图满足相邻通孔最小间距约束的布线方法”专利获授权
汇顶科技“打码控制及打码方法、系统、芯片、电子设备及存储介质”专利获授权
公司新闻:北京佰司特中标中标大连理工大学超高速视频级原子力显微镜采购项目
公司新闻:北京佰司特签约韩国Sol Inc. 公司的全自动细胞计数仪SOL COUNT
公司新闻:北京佰司特贸易有限责任公司中标 北京生命科学研究所质谱招标采购项目(国内第一台质量光度计二
创新引领 YOUNG帆起航——仪器信息网25周年 我们不一YOUNG!